Применение радиочастотной абляции вагинального канала при генитоуринарном синдроме в менопаузе
Роджер Ротенбергер1, Элейн Копинга2, Джеффри Делл3, Роберт Д. Мур4, Джон Р. Миклош4, Микки Каррам5
1 Отделение акушерства и гинекологии и женского здоровья, отдел женской тазовой медицины и реконструктивной хирургии, Медицинский центр Университета Луисвилля, Луисвилль, Кентукки, США
2 Калифорнийский центр женского тазового здоровья и сексуального благополучия, Корона-дель-Мар, Калифорния, США
3 Институт женской тазовой медицины, Ноксвилл, штат Теннесси, США
4 Урогинекология и косметическая вагинальная хирургия Миклоша и Мура, Альфаретта, Джорджия, США
5 Отделение женской тазовой медицины и реконструктивной хирургии, Больница Христа, Либерти Тауншип, Огайо, США
Абстракт
История вопроса. Генитоуринарный синдром в менопаузе (ГУСМ) — распространенное заболевание с целым комплексом симптомов, включающим в себя жжение, сухость, диспареунию и ирритативные симптомы нижних мочевых путей, которые возникают в результате атрофических изменений вульвовагинальной области. Хотя гормональная терапия является основным методом лечения ГУСМ, некоторые пациентки могут прибегнуть к негормональным методам лечения. Цель — определить эффективность радиочастотной (radiofrequency; RF) абляции вагинального канала с помощью аппликатора MorpheusV для уменьшения симптомов ГУСМ. Методы. Мы провели многоцентровую проспективную серию исследований женщин с ГУСМ по индексу вагинального здоровья (Vaginal Health Index Score; VHIS). Участницы получили 3 процедуры RF-абляции с интервалом примерно в 4 нед и последующим наблюдением в течение 6 мес после процедуры. Исходы. Первичной конечной точкой была оценка по VHIS через 6 мес после лечения. Вторичными конечными точками были оценка VHIS через 3 мес, оценки боли по визуальной аналоговой шкале (ВАШ) при каждом терапевтическом визите, 3- и 6-месячного по реестру урогенитального дистресса — 6 (Urogenital Distress Inventory-6; UDI-6) и индексу женской сексуальной функции (Female Sexual Function Index; FSFI). Результаты. С 2021 по 2023 г. в исследование была включена 71 женщина, 51 из них наблюдалась до 6 мес. Результаты лечения показали низкий уровень боли по шкале ВАШ со средними значениями 2,13 ± 2,1, 2,55 ± 2,38 и 2,18 ± 2,14 при терапевтических визитах 1, 2 и 3 соответственно. Улучшение показателей по шкале VHIS наблюдалось с исходного уровня до 3 мес после лечения (15,00 ± 5,37 против 19,62 ± 4,44) и сохранялось в течение 6 мес (20,23 ± 4,12) (P < 0,001). Также было отмечено значительное улучшение показателей UDI-6 и FSFI между исходным уровнем и через 6 мес после лечения (FSFI: 18,81 ± 9,57 против 22,81 ± 10,34, P < 0,001; UDI-6: 39,58 ± 15,98 против 22,42 ± 14,03, P < 0,001). В ходе исследования ни у одной участницы не возникло побочных явлений. Клинические последствия. Безопасная и эффективная терапия ГУСМ и симптомов нижних мочевых путей без использования гормональных методов имеет большое клиническое значение для многих пациенток, которые не могут или не хотят принимать эти препараты. Сильные стороны и ограничения. К достоинствам данного исследования относится использование 3 сеансов лечения, а также наблюдение за участницами до 6 мес после лечения с комплексной оценкой симптомов. К ограничениям относятся неслепой характер исследования и отсутствие группы сравнения. Заключение. Данные представленного исследования свидетельствуют о том, что RF-абляция вагинального канала с помощью аппликатора MorpheusV является безопасным и эффективным вмешательством при ГУСМ. Кроме того, показано субъективное улучшение стрессового недержания мочи, ургентного недержания мочи и сексуальной функции.
Ключевые слова: вульвовагинальная атрофия, генитоуринарный синдром в менопаузе, радиочастотная терапия, RF-терапия, MorpheusV, стрессовое недержание мочи, ургентное недержание мочи
Введение
Генитоуринарный синдром в менопаузе (ГУСМ) — это симптомокомплекс, состоящий из жжения, сухости, диспареунии и ирритативных симптомов нижних мочевых путей, которые возникают в результате атрофических изменений вульвовагинальной области. Эти симптомы часто прогрессируют и затрагивают 27–84% женщин в постменопаузе [1, 2]. Вагинальная эстрогенная терапия эффективна в лечении ГУСМ [3–5]. Но некоторые женщины могут иметь противопоказания к использованию эстрогенов, а другие просто хотят избежать применения гормональных препаратов [1, 4]. Именно поэтому необходимы негормональные методы лечения этого очень распространенного и мучительного состояния.
Первым энергетическим методом лечения вагинальной дисфункции, который был изучен и мог оказывать влияние на ГУСМ, является фракционный CO2-лазер [6–9]. Предполагаемый механизм действия заключается в том, что световая энергия вызывает воспалительную реакцию, в результате которой высвобождаются фибробласты, стимулирующие выработку коллагена в расслоившемся сквамозном эпителии. В процессе выработки коллагена образуются мелкие капилляры, которые снабжают коллагеновую ткань кровью, создавая транссудат, обеспечивающий смазку влагалищного канала. Со временем стенки влагалища утолщаются, а рН влагалища становится более кислым, поскольку в нем снова появляются лактобактерии и гликоген [10].
Серии случаев нерегулярно демонстрировали положительный эффект у пациенток с ГУСМ; однако в недавнем рандомизированном контролируемом исследовании лазер не был значительно лучше, чем фиктивное лечение [8]. Сегодня для лечения лица и тела стали доступны устройства для радиочастотной (radiofrequency; RF) микроигольчатой терапии. В недавно опубликованном исследовании описано первое устройство для микроигольчатой терапии, используемое в вагинальном канале (MorpheusV), отмечена его безопасность и хорошая краткосрочная эффективность при лечении ГУСМ [11].
В отличие от световой терапии (лазера) с проникновением в эпителий влагалища на 750 микрон, RF-энергия при микроигольчатой терапии проникает на глубину до 3 мм. Глубина воздействия имеет большое значение, поскольку предыдущие исследования, проведенные на лице и теле, показали, что RF-энергия, подаваемая на глубину 0,5–3,5 мм, способствует превосходному дополнительному неоколлагеногенезу по сравнению с поверхностным ее применением [11]. Кроме того, в результате неинвазивной RF-терапии в некоторых исследованиях было показано улучшение функции мочевого пузыря [2, 8 , 12, 13].
Это потенциальное улучшение мочевых симптомов особенно заметно в популяции с ГУСМ, учитывая, что пациентки, страдающие ГУСМ, обычно имеют ассоциацию дисфункции мочевого пузыря и женской сексуальной дисфункции [14–16].
Целью данного исследования было определить, во-первых, эффективность RF-абляции вагинального канала с помощью аппликатора MorpheusV для уменьшения симптомов ГУСМ, во-вторых, влияние этой терапии на мочевой пузырь и сексуальную функцию.
Методы
Данная работа представляет собой проспективную серию историй болезни женщин, набранных из двух клиник в период с июня 2021 по январь 2023 г.
Критерии включения в исследование:
- женщины в постменопаузе (возрасте 35–75 лет) с отсутствием менструаций не менее 12 мес;
- индекс массы тела меньше или равный 36;
- готовность участниц воздерживаться от других методов лечения ГУСМ и недержания мочи в течение как минимум 6 мес.
Критерии исключения:
- наличие в анамнезе кардиостимулятора или внутриполостного дефибриллятора, любого другого активного электрического имплантата в любом месте тела, а также постоянных имплантатов в обрабатываемой области;
- тяжелые сопутствующие заболевания, такие как кардиологические, неврологические, эндокринные, иммунные, печеночные или почечные расстройства;
- временной период не менее 3 мес с момента предыдущей операции в области лечения;
- временной период не менее 6 мес после любых других недавних процедур, таких как световое, CO2-лазерное или RF-лечение в области воздействия;
- 30 дней после лечения любым вагинальным эстрогенным препаратом.
Участницы также не должны были в течение 6 мес принимать какие-либо препараты или проходить процедуры, связанные с ургентным недержанием мочи. Участницы с активной инфекцией мочевых путей или генитальной инфекцией исключались.
Первичным результатом была объективная оценка атрофии/эстрогенизации влагалища, измеренная с помощью глобально валидированного индекса вагинального здоровья (Vaginal Health Index Score; VHIS) через 6 мес. VHIS представляет собой комбинацию пяти субшкал, измеряемых от 1 (хуже) до 5 (лучше): эластичность, объем выделений, pH, целостность эпителия и увлажненность. При использовании версии G∗Power 3.1.9.7 (2020 г.) и с учетом приведенных ниже допущений потребовался объем выборки в 28 пациентов, чтобы выявить средний размер эффекта (0,25) при мощности 80% с использованием метода дисперсионного анализа повторных измерений (analysis of variance; ANOVA) с тремя периодами измерения при α = 0,05, корреляции между повторными измерениями 0,05 и с поправкой на несферичность 1,00.
Вторичные результаты также включали оценку по опроснику VHIS на исходном уровне и через 3 мес, оценку боли/дискомфорта, испытываемых во время лечения, по 10-балльной визуальной аналоговой шкале (ВАШ) сразу после процедуры. Влияние лечения на сексуальную функцию оценивалось с помощью индекса женской сексуальной функции (Female Sexual Function Index; FSFI) на исходном уровне и через 3 и 6 мес. Также были собраны измерения по реестру урогенитального дистресса — 6 (Urogenital Distress Inventory-6; UDI-6) на исходном уровне, через 3 и 6 мес. Сроки сбора данных в зависимости от времени поступления и лечения приведены в табл. 1.
Участницы заполняли форму информированного согласия перед проведением любых процедур исследования. Сначала участницы явились в клинику для скринингового визита, чтобы определить возможность участия в исследовании. Опросы проводились в соответствии с табл. 1. Были собраны демографические данные, включая пол, возраст, расу и тип кожи (шкала Фицпатрика). Шкала Фицпатрика — это числовая система классификации, используемая для определения цвета кожи в зависимости от ее реакции на воздействие ультрафиолетового света [17].
Таблица 1. Сроки сбора данных в зависимости от времени поступления и лечения
| Визит
Тип |
Базовые скрининговые показатели | Визит 1*
Tx1 |
Визит 2
Tx2 (4 нед ± 5 дней) |
Визит 3
Tx3 (4 нед ± 5 дней) |
Визит 4
Наблюдение через 3 мес (± 7 дней) |
Визит 5
Наблюдение через 6 мес (± 14 дней) |
| История болезни и демографические данные | √ | |||||
| Критерии включения/исключения | √ | |||||
| Информированное согласие | √ | |||||
| Лечение | √ | √ | √ | |||
| FSFI | √ | √ | √ | |||
| Показатель «Индекс вагинального здоровья» (VHIS) | √ | √ | √ | |||
| UDI-6 | √ | √ | √ | |||
| Запрос о нежелательных явлениях | √ | √ | √ | √ | √ | |
| Оценка уровня дискомфорта | √ | √ | √ | |||
| Сопутствующие препараты | √ | √ | √ | √ | √ | √ |
| Окончание исследования |
*Обследование и лечение могут проводиться в один и тот же день с интервалом до 3 нед.
Участницы в этом исследовании проходили лечение с помощью системы InMode с аппликатором MorpheusV. Система InMode с аппликатором MorpheusV предназначена для фракционной доставки RF-энергии в кожу через матрицу из 24 контактных электродов. Такая доставка RF-энергии была ранее описана в работе Abdelaziz A. и соавт. В данном исследовании, как и в работе Abdelaziz A. и соавт., применяется вагинальная RF-терапия с идентичной мощностью и глубиной лечебного воздействия. Это предыдущее исследование продемонстрировало безопасность и краткосрочную эффективность в популяции с ГУСМ [11].
Мощность RF-энергии составляет менее 5% от общей площади обработки. Во время лечения RF-ток проходит между матрицей игольчатых электродов и возвратным электродом, оказывая наибольшее воздействие с кончиков игольчатых электродов, где он создает небольшую зону коагуляции в коже. Верхняя часть каждого электрода покрыта изолирующим материалом (парилен) для минимизации воздействия на эпидермис и доставки RF-энергии только от дистального края микроиглы длиной 0,5 мм в более глубокие слои кожи.
Все участницы получили 3 процедуры с использованием аппликатора MorpheusV с интервалом примерно в 4 нед и последующим наблюдением до 6 мес (общие временные точки включают исходный уровень, терапевтическую процедуру 1 (treatment 1; Tx1), процедуру 2 (Tx2) и процедуру 3 (Tx3), наблюдение через 3 мес и наблюдение через 6 мес. Анестезия перед процедурой достигалась путем нанесения крема, содержащего 23% лидокаин / 7% тетракаин, на область обработки на 25 мин. Область воздействия включала весь вагинальный канал, преддверие, заднюю спайку малых половых губ и верхнюю часть промежности. Частота RF-излучения составляла 1 МГц, мощность — 30–35 Вт. Вводился аппликатор MorpheusV, и импульсы доставляли методом штамповки, вращая аппликатор, на одну и ту же глубину в 5 точках на 9:00, 10:30, 12:00, 1:30 и 3:00, 4:30, 6:00 и 7:30, пока не будет пройден полный круг (360°). Затем аппликатор вытягивался на 1 см, и повторялось вращение с импульсами. Этот процесс повторялся до тех пор, пока электроды аппликатора не оказывались у интроита (входа во влагалище). Все пациентки получали лечение на глубине введения микроигольчатых электродов 3 мм, затем 2 мм, затем 1 мм на каждом сеансе — от 450 до 600 импульсов. Нежелательные явления оценивались во время всех сеансов лечения и последующих визитов.
Все показатели измерялись на исходном уровне, через 3 и 6 мес. Применялся метод дисперсионного анализа повторных измерений (ANOVA). Парные сравнения использовались по мере необходимости для сравнения переменных до и после лечения; применялась поправка Бонферрони на множественные сравнения. Для всех статистических анализов использовалось программное обеспечение SPSS (IBM SPSS Statistics for Windows; v. 22, IBM Corp., 2013).
Результаты
В общей сложности с июня 2021 по январь 2023 г. в двух центрах в исследование для определения эффективности аппликатора MorpheusV при симптомах ГУСМ были включены 72 женщины. Из 72 пациенток, включенных в программу, только 50 наблюдались до 6 мес. Средний возраст составил 55,96 (SD = 10,53), минимальный возраст — 37 лет, максимальный — 77 лет. По типу кожи (шкала Фицпатрика) 31% имели II фототип кожи, 53% — III фототип, 14% — IV фототип и 2% — VI фототип кожи. Что касается расовой принадлежности, то 2% были афроамериканками, 90% — представительницами европеоидной расы и 4% — латиноамериканками; расовая принадлежность двух пациенток не была определена (4%) (табл. 2).
Таблица 2. Демографические данные участниц
| Среднее | Минимум | Максимум | |||
| Возраст | 55,96 ± 10,53 | 37 | 77 | ||
| Шкала Фицпатрика | Тип I
0% |
Тип II
31% |
Тип III
53% |
Тип IV
0% |
Тип V
14% |
| Раса | Афроамериканки
2% |
Европеоидная раса
90% |
Латиноамериканки
4% |
Не идентифицировано
4% |
В зависимости от измерения анализ проводился с использованием данных 47–50 пациенток, начиная с исходного уровня и до 6 мес после лечения (исходный уровень, Tx1, Tx2 и Tx3, наблюдение через 3 мес и наблюдение через 6 мес). Во время сбора данных, если какой-либо элемент данных отсутствовал, данные из всех других временных точек удалялись. В связи с этим количество пациенток для каждого инструмента было следующим: шкала боли ВАШ — N = 47, VHIS общий — N = 47, VHIS эластичность — N = 50, VHIS объем выделений — N = 50, VHIS pH — N = 48, VHIS целостность эпителия — N = 50, VHIS увлажненность — N = 50, FSFI — N = 49 и UDI-6 — N = 50.
Пациенток просили оценить боль после каждой процедуры по 10-балльной шкале ВАШ (ниже — менее болезненно) [18]. Пациентки отметили, что уровень боли был значительно ниже медианного значения 5, а результаты повторного теста ANOVA показали, что боль существенно не различалась при каждой процедуре: Tx1 среднее = 2,13 (SD = 2,10), Tx2 среднее = 2,55 (SD = 2,38) и Tx3 среднее = 2,18 (SD = 2,14); F(2, 92) = 0,92, P = 0,40. Другими словами, пациентки считали, что процедуры были качественно не болезненными, и эта оценка не менялась от процедуры к процедуре.
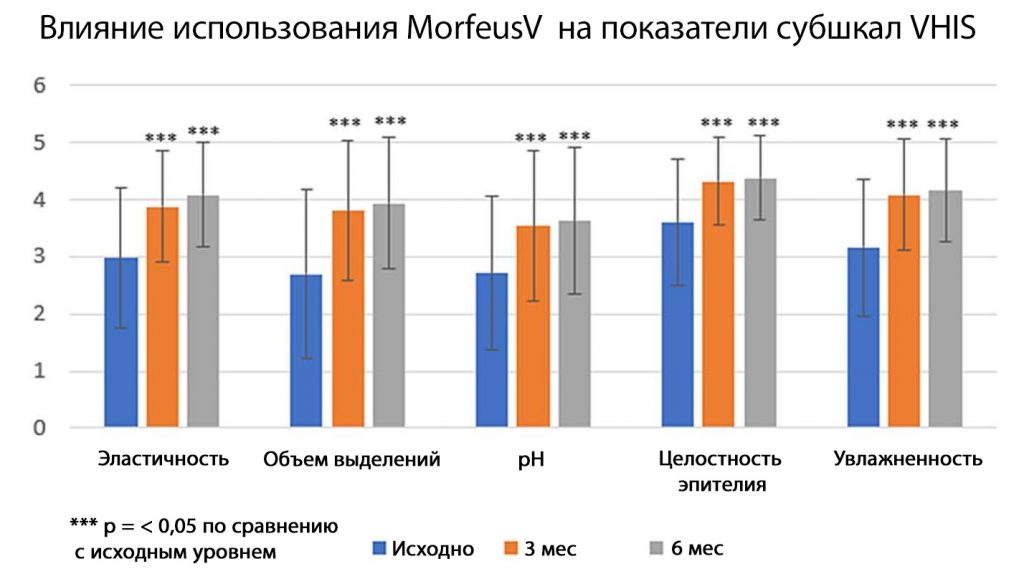
Рис. 1. Показатели VHIS, UDI-6 и FSFI на исходном уровне в сравнении с показателями через 3 и 6 мес после радиочастотной микроигольчатой терапии MorpheusV
Показатели VHIS определялись на исходном уровне, а также при наблюдении через 3 и 6 мес (рис. 1). Тест ANOVA оказался статистически значимым — F(2, 92) = 48,32, P < 0,001, при этом исходное среднее значение было самым низким (m = 15,00, SD = 5,37), увеличивалось к через 3 мес (m = 19,62, SD = 4,44) и оставалось стабильным через 6 мес наблюдения (m = 20,23, SD = 4,12). Анализ парных сравнений демонстрирует, что исходный уровень отличается от измерений через 3 и 6 мес (P < 0,001); кроме того, данные VHIS через 3 и 6 мес статистически достоверно отличаются друг от друга (P < 0,05), что указывает на то, что показатель VHIS улучшается к 3 мес и продолжает улучшаться через 6 мес.

Рис. 2. Эластичность, объем выделений, рН, целостность эпителия и увлажненность кожи на исходном уровне, а также через 3 и 6 мес после лечения с указанием стандартных отклонений
Результаты измерений по отдельным субшкалам VHIS представлены на рис. 2. При тестировании ANOVA всех субшкал VHIS разница между исходным уровнем, через 3 мес и через 6 мес была статистически значимой (P < 0,001), хотя средние значения за 3 мес и 6 мес не различались.
Показатели FSFI в целом значительно улучшились. Тестирование FSFI ANOVA было статистически значимым — F(2, 96) = 12,57, P < 0,001, при этом исходное среднее значение было самым низким (m = 18,81, SD = 9,57), увеличилось до высокого уровня через 3 мес наблюдения (m = 22,61, SD = 10,32) и сохранилось на этом уровне через 6 мес наблюдения (m = 22,81, SD = 10,34) (см. рис. 1). Анализ парных сравнений демонстрирует, что исходный уровень отличается от измерений через 3 и 6 мес (P < 0,01). Кроме того, значения через 3 и 6 мес статистически не отличаются друг от друга, что указывает на то, что показатель FSFI улучшается к 3 мес и сохраняет это улучшение через 6 мес. Более того, на исходном уровне 70% пациенток с данными 6-месячного наблюдения были сексуально дисфункциональными по шкале FSFI (значение меньше или равно 26). Через 6 мес сексуальная дисфункция сохранялась только у 48% этих пациенток.
Наконец, данные тестирования UDI-6 ANOVA оказались статистически значимым — F(2, 98) = 43,92, P < 0,001, при этом исходное среднее значение было самым высоким (m = 39,58, SD = 15,98), снижалось к 3 мес наблюдения (m = 22,50, SD = 14,85) и оставалось стабильным к 6 мес наблюдения (m = 22,42, SD = 14,03) (см. рис. 1). Анализ парных сравнений демонстрирует, что исходный уровень отличается от результатов измерений через 3 и 6 мес (P < 0,001); однако данные через 3 и 6 мес статистически не отличаются друг от друга, что указывает на то, что показатель UDI-6 улучшается к 3 мес и сохраняет это улучшение через 6 мес. Более того, на исходном уровне 67% пациенток с данными 6-месячного наблюдения имели аномальные показатели UDI-6 (значение больше или равно 33,33). Через 6 мес только 26% этих пациенток имели отклонения от нормы по UDI-6.
В течение 6 мес ни у одной участницы не было зарегистрировано побочных явлений.
Обсуждение
В данном исследовании мы оценили эффективность микроигольчатой RF-терапии в лечении ГУСМ с помощью аппликатора MorpheusV. Процедура хорошо переносилась. Болевые ощущения были незначительными и составляли около 2 баллов по шкале ВАШ при каждой процедуре.
Участницы продемонстрировали значительное улучшение показателей VHIS, а средние показатели VHIS через 3 и 6 мес превысили пороговое значение VHIS для ГУСМ — 15 (среднее значение за 3 мес — 19,62, SD = 4,44, среднее значение за 6 мес — 20,23, SD = 4,12). Все показатели VHIS (эластичность, объем выделений, рН, целостность эпителия и увлажненность) при тестировании ANOVA улучшились по сравнению с исходным уровнем, но не улучшились между 3 и 6 мес (рис. 2).
Дисфункция мочевого пузыря часто сопровождает ГУСМ и играет важную роль в качестве жизни. Влияние вагинальной RF-терапии на недержание, затрудненное мочеиспускание и дискомфорт при мочеиспускании оценивалось по шкале UDI-6. Показатель UDI-6 значительно снизился через 3 мес и сохранился через 6 мес. Более того, исходный средний показатель UDI-6 был выше порогового значения 33,33, свидетельствующего о расстройстве мочеиспускания, в то время как средние значения через 3 и 6 мес были ниже этого порога. Это указывает на то, что RF-аппликатор MorpheusV эффективен для улучшения мочевых симптомов до 6 мес после процедуры.
Сексуальная функция также часто страдает от ГУСМ. Влияние на сексуальную функцию оценивалось с помощью опросника FSFI, который показал значительное улучшение с исходного уровня к 3 мес после последнего курса лечения (18,81 ± 9,57 против 22,61 ± 10,32), которое сохранялось и через 6 мес (22,81 ± 10,34).
Стандартное лечение ГУСМ включает в себя использование вагинальных эстрогенов. Поскольку многие женщины имеют относительные или абсолютные противопоказания к применению эстрогенсодержащих препаратов, крайне необходимо найти успешное негормональное адекватное лечение этого распространенного расстройства.
Использование фракционного CO2-лазера в лечении ГУСМ было показано в многочисленных сериях случаев для улучшения симптомов ГУСМ, но не продемонстрировало значительного влияния на функцию мочевого пузыря. Это может быть связано с тем, что воздействие энергетических процедур ограничено областями, где применяется энергия при лазерной терапии. Вероятно, фракционные CO2-лазерные зонды фокусируются на самом влагалище и направленно не воздействуют на уретральное отверстие или ткани, непосредственно связанные с функцией мочевого пузыря [2, 6, 8, 10, 12, 13, 19–21]. Мы считаем, что вагинальный эпителий будет реагировать на тепловую (RF) и световую (лазер) энергию аналогичным образом. Кроме того, мы предполагаем, что наши результаты и улучшение функции мочевого пузыря могут быть обусловлены более глубоким проникновением в эпителий влагалища (3 мм против 750 микрон), а также более эффективной обработкой вагинального канала. Такая более эффективная обработка при RF-терапии обусловлена техникой штамповки с тремя перекрывающимися зонами обработки, в результате чего обрабатывается гораздо бо́льшая площадь поверхности вагинального канала по сравнению с ручным вращением зонда при лазерной обработке.
Кроме того, в этом исследовании отмечено значительное улучшение дисфункции нижних мочевых путей, которая обычно ассоциирует с ГУСМ. Теоретически это может быть связано с уменьшением рецидивирующего цистита из-за изменения среды влагалища или с изменением среды за счет восстановления кислотности вульвовагинальной области.
Это второе исследование, посвященное данному методу терапии [11]. В представленном исследовании использовалось 3 сеанса лечения, за пациентками наблюдали в течение 6 мес после лечения, а симптомы оценивались комплексно. Авторы, однако, признают, что у этого исследования есть существенные ограничения. Оно не было слепым и не имело группы сравнения. Будущие исследования должны включать рандомизированные слепые плацебо-контролируемые испытания с более длительным периодом наблюдения.
Заключение
В представленном исследовании отмечено значительное улучшение результатов ГУСМ-обследования, сексуальной функции и функции мочевого пузыря. Также отмечены отсутствие каких-либо побочных явлений и высокая степень удовлетворенности. Именно в таком контексте следует рассмотреть возможность продолжения исследований по использованию RF-терапии в при лечении ГУСМ.
Литература
- The NAMS 2020 GSM Position Statement Editorial Panel. The 2020 genitourinary syndrome of menopause position statement of the North American Menopause Society. Menopause 2020; 27(9): 976–992.
- Jang Y., Leung C.Y., Huang H. Comparison of severity of genitourinary syndrome of menopause symptoms after carbon dioxide laser vs vaginal Estrogen therapy a systematic review and meta-analysis. JAMA Netw Open 2022; 5(9): 1–11.
- Nappi R.E., Palacios S., Bruyniks N., et al. Study investigators. The burden of vulvovaginal atrophy on women’s daily living: Implications on quality of life from a face-to-face real-life survey. Menopause 2019; 26(5): 485–491.
- Lethaby A., Ro A., Roberts H. Local oestrogen for vaginal atrophy in postmenopausal women (review). Cochrane Database Syst Rev 2016; 2016(8): CD001500.
- ACOG Practice Bulletin No. 141: management of menopausal symptoms. Obstet Gynecol 2014; 123(1): 202–216.
- Goldstein S.W., Goldstein I., Kim N.N., et al. Safety and efficacy of fractional CO2 laser treatment to the vestibule: a randomized, double-blind, sham-controlled, prospective 3-site clinical study in women with vestibular pain. J Sex Med 2023; 20(6): 800–812.
- Filippini M., Porcari I., Ruffolo A.F., et al. CO2-laser therapy and genitourinary syndrome of menopause: a systematic review and meta-analysis. J Sex Med 2022; 19(3): 452–470.
- Li F.G., Fuchs T., Deans R., et al. Vaginal epithelial histology before and after fractional CO2 laser in postmenopausal women: a double-blind, sham-controlled randomized trial. Am J Obstet Gynecol 2023; 229(3): 278.e1–278.e9.
- Li F.G., Maheux-Lacroix S., Deans R., et al. Effect of fractional carbon dioxide laser vs sham treatment on symptom severity in women with postmenopausal vaginal symptoms: a randomized clinical trial. J Am Med Assoc 2021; 326(14): 1381–1389.
- Jugulyte N., Zukiene G., Bartkeviciene D. Emerging use of vaginal laser to treat genitourinary syndrome of menopause for breast cancer survivors: a review. Medicina (Kaunas) 2023; 59(1): 132–143.
- Abdelaziz A., Blusewicz T.A., Coley K.P., Karram M. Safety, tolerability and short-term efficacy of transvaginal fractional bipolar radiofrequency therapy for symptoms of stress and or mixed in continence in conjunction with genitourinary syndrome of menopause. Neurourol Urodyn 2023; 42(4): 807–813.
- Gunter J. Genitourinary syndrome of menopause and the false promise of vaginal laser therapy. JAMA Netw Open 2023; 6(2): e2255706.
- Di D.V., Oria O.D., Giannini A., et al. The efficacy of fractional CO2 laser in the treatment of genitourinary syndrome of menopause: a large prospective observational study. Clin Exp Obstet Gynecol 2022; 49(9): 212.
- Gandhi J., Chen A., Dagur G., et al. Genitourinary syndrome of menopause: an overview of clinical manifestations, pathophysiology, etiology, evaluation, and management. Am J Obstet Gynecol 2016; 215(6): 704–711.
- Rahn D.D., Carberry C., Sanses T.V., et al. Vaginal Estrogen for genitourinary syndrome of menopause. Obstet Gynecol 2014; 124(6): 1147–1156.
- Hyun H.-S., Park B.-R., Kim Y.-S., et al. Urodynamic characterization of postmenopausal women with stress urinary incontinence: retrospective study in incontinent pre- and post-menopausal women. J Korean Soc Menopause 2010; 16(3): 148–152.
- Fitzpatrick T.B. The validity and practicality of sun-reactive skin types I through VI. Dermatol Clin 1992; 10(2): 235–238.
- Andres M.P., Coelho L.G., Riccio H., et al. Visual analogue scale cut-off point of seven represents poor quality of life in patients with endometriosis. Reprod Sci 2024; 31(4): 1146–1150.
- Pessoa L.L.M.N., Sarmento A.C.A., Medeiros K.S., et al. Efficacy and safety of laser therapy for the treatment of genitourinary syndrome of menopause: a protocol for systematic review and meta-analysis of clinical trials. Front Reprod Health 2021; 3: 772690–772690.
- Knight C, Logan V, Fenlon D. A systematic review of laser therapy for vulvovaginal atrophy / genitourinary syndrome of menopause in breast cancer survivors. eCancer 2019; 13(988).
- Schachar J.S., Devakumar H., Martin L., et al. Prospective study of fractional carbon dioxide laser therapy for symptoms of genitourinary syndrome of menopause : one-year follow-up. J Clin Gynecol Obstet 2021; 10(1): 11–17.
